Alla kliniska studier kräver etikgodkännande. Sammanställningen nedan baseras på data i Etikprövningsmyndighetens årsredovisningar, som håller aggregerad information om hur många ärenden som hanterats, och på data från ett utdrag från myndighetens diarium för åren 2020–2022.
Sammanställningarna visar vilken typ av analyser som går att göra med vilken data. För att få en ökad förståelse för den planerade forskningen och för enskilda studier behövs dock ytterligare information. Etikprövningsmyndigheten har ett pågående uppdrag att samla och presentera statistik över kliniska studier i Sverige och när kompletterande och mer detaljerad information blir tillgänglig blir det möjligt att göra djupare analyser.
Inkomna etikprövningsansökningar
Antalet inkomna etikprövningsansökningar som avser kliniska studier ligger vanligtvis i intervallet 2 200–2 400 ansökningar per år. Sedan 2022 redovisas kliniska läkemedelsprövningar som hanteras enligt den nya EU-förordningen om kliniska prövningar för humanläkemedel, som en egen kategori (CTR) i årsredovisningarna.
Etikprövningsmyndighetens årsredovisningar innehåller även information om antal ändringsansökningar. Denna kategori uppgår till närmare 3 000 per år vilket är över 50 procent av totala mängden ärenden. Ändringsansökningar är inte unika studier utan handlar om redan påbörjade studier och kan exempelvis bero på att forskaren vill göra lägga till fler deltagande kliniker (studiesite) eller samla in ytterligare data utöver det som framgått av det ursprungliga etiktillståndet.
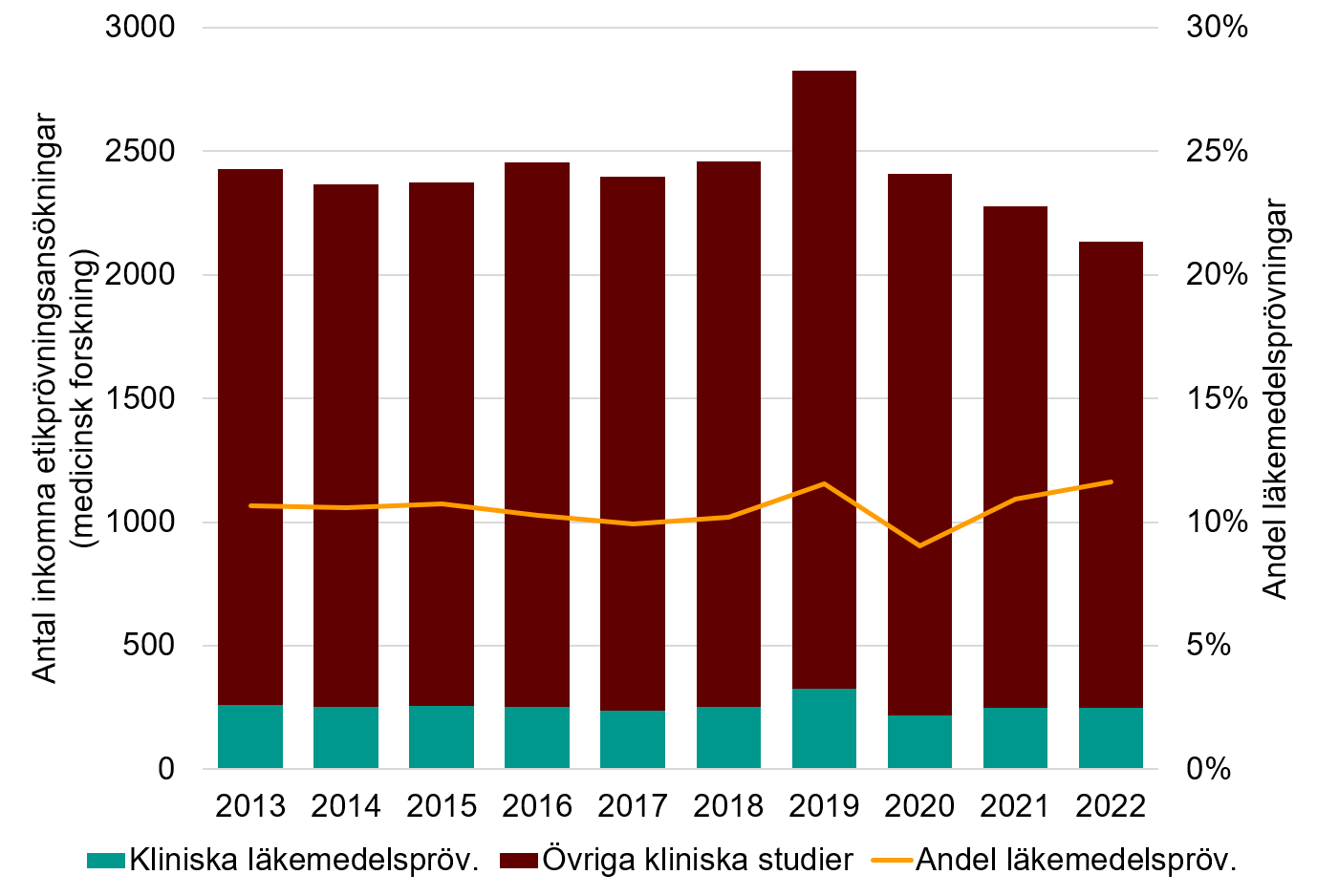
Figur 1. Inkomna etikprövningsansökningar som avser medicinsk forskning enligt årsredovisningarna för de regionala etikprövningsnämnderna (2013-2018) och Etikprövningsmyndigheten (2019-2022), uppdelat på kliniska läkemedelsprövningar och övriga medicinska ansökningar (kliniska studier). Ökningen 2019 kan vara en effekt av dubbelräkning av enstaka ansökningar vid övergången från de tidigare regionala etikprövningsnämnderna till den nya Etikprövningsmyndigheten. 2022 har ansökningarna enligt den nya EU-förordningen (CTR) inkluderats i kategorin läkemedelsprövningar.
Kliniska läkemedelsprövningar | Övriga medicinka ansökningar | Andel kliniska läkemedelprövningar | |
|---|---|---|---|
2013 | 259 | 2170 | 11% |
2014 | 251 | 2117 | 11% |
2015 | 255 | 2120 | 11% |
2016 | 252 | 2205 | 10% |
2017 | 238 | 2160 | 10% |
2018 | 251 | 2210 | 10% |
2019 | 326 | 2501 | 12% |
2020 | 218 | 2190 | 9% |
2021 | 249 | 2030 | 11% |
2022 | 248,5 | 1887 | 12% |
Andel godkända etikprövningsansökningar
En hög andel av alla ansökningar till Etikprövningsmyndigheten blir godkända. Under 2020–2022 blev 94 procent av alla ansökningar som avser medicinsk forskning godkända, vilket motsvarar cirka 2000 ansökningar varje år. Två procent fick avslag och resterande är framförallt ansökningar som dras tillbaka av sökande eller avvisas för att ansökan inte faller under etikprövningslagen.
Nästan all forskning får alltså godkänt att starta men det saknas heltäckande statistik över hur många av studierna som faktiskt påbörjas, hur många forskningspersoner som inkluderas i studierna och över hur många studier som avslutats.
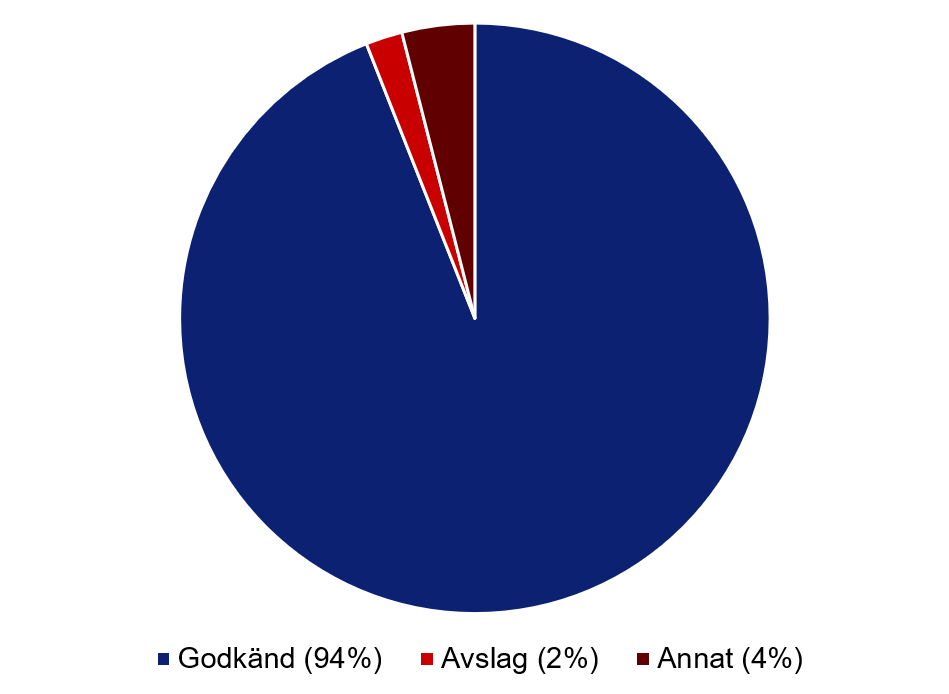
Figur 2. Fördelning av beslut för etikprövningsansökningar under 2020–2022 som avser kliniska studier (medicinsk forskning). I kategorin ”annat” hamnar framförallt ärenden som dras tillbaka av sökande eller avvisas för att ärendet inte faller under etikprövningslagen. Ändringsansökningar eller ärenden som resulterar i rådgivande yttranden har exkluderats.
Medicinsk ärendetyp | |
|---|---|
Godkänd | 94% |
Avslag | 2% |
Annat | 4% |
Geografisk fördelning av godkända etikprövningsansökningar
Huvudmän i Stockholms sjukvårdsregion står som ansvariga för ungefär en tredjedel av alla etikprövningsansökningar som godkänns. Därefter följer sjukvårdsregion Mellansverige och Västra sjukvårdsregionen med runt 18 respektive 17 procent vardera. I förhållande till storleken på befolkningen (enligt befolkningsstatistik från SCB, 31 december 2022) i respektive sjukvårdsregion har Stockholm en högre andel medan återstående sjukvårdsregioner har en mindre andel i förhållande till sin befolkningsandel.
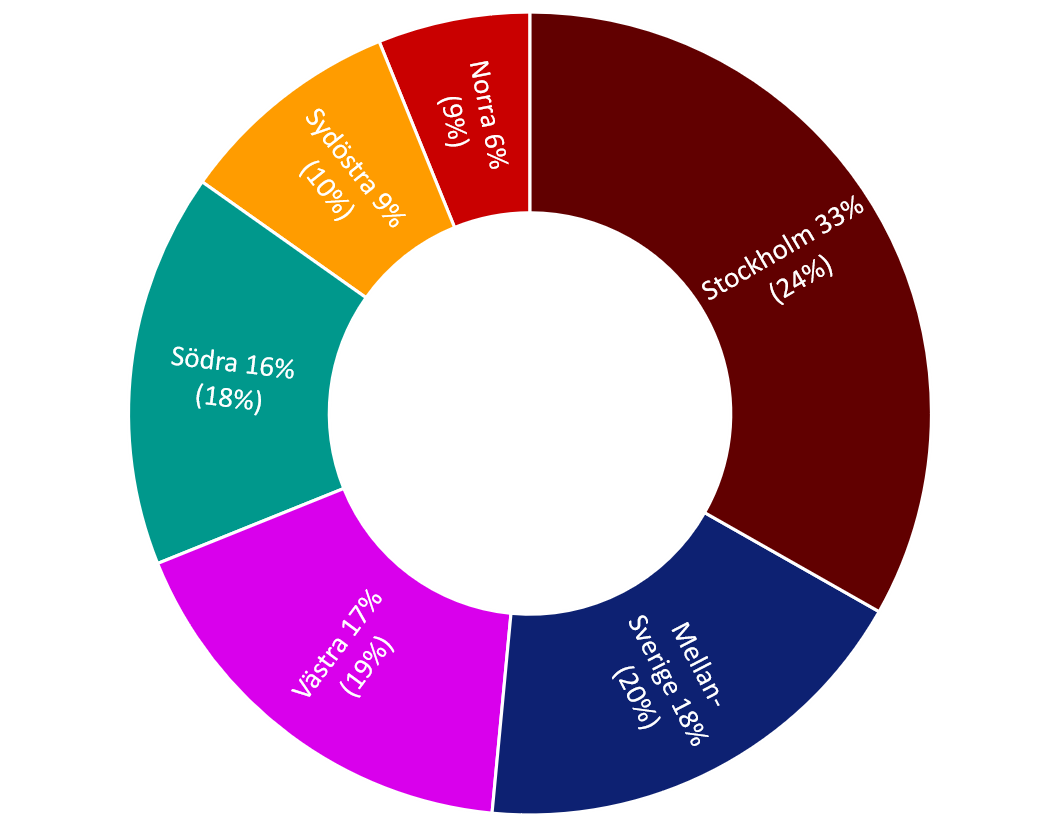
Figur 3. Geografisk fördelning av godkända etikprövningsansökningar som avser kliniska studier (medicinsk forskning) under 2020-2022. Siffran inom parentes visar befolkningsandelen för respektive sjukvårdsregion.
Andel ansökningar | Befolkningsandel | |
|---|---|---|
| Norra | 6% | 9% |
Mellansverige | 18% | 20% |
Stockholm | 33% | 24% |
Sydöstra | 9% | 10% |
Västra | 17% | 19% |
Södra | 16% | 18% |
Fördelning av etikprövningsansökningar utifrån avgiftskategori
Etikprövningsmyndighetens avgiftskategorier ger en indikation på vilken typ av studier som planeras. Kliniska läkemedelsprövningar står för 11 procent av ansökningarna och medicintekniska kliniska prövningar för 1 procent (fördelningen är baserad på ansökningar mellan åren 2020–2022). Kategorin ”Behandling av personuppgifter” utgör 32 procent av ansökningarna och kan till stor del antas vara studier som använder data som genererats inom vården. Övriga kliniska studier är enbart klassade utifrån antal huvudmän som medverkar och därmed går det inte att göra djupare analyser kring studietyper. Få studier har forskningspersoner från flera sjukvårdsregioner*. Senaste ALF-utvärderingen belyser att svensk klinisk forskning skulle gynnas av fler nationella samarbeten, men att vissa regioner inom vissa forskningsområden idag konkurrerar snarare än samverkar.
* Det är framförallt avgiftskategori B där det är tydligt att samverkan mellan forskningshuvudmän sker. Det behövs kompletterande information om medverkande huvudmän för samtliga ansökningar för att kunna göra en djupare analys kring mängden samverkan för exempelvis avgiftskategori D och E.
Avgiftskategori | Andel ansökningar |
|---|---|
En forskningshuvudman (A) | 43% |
Flera forskningshuvudmän (B) | 7% |
Flera forskningshuvudmän, men där forskningspersonerna är kopplade till en forskningshuvudman (C) | 7% |
Behandling av personuppgifter (D) | 32% |
Klinisk läkemedelsprövning (E + CTR) | 11% |
Medicinteknik (MDR + IVDR) | 1% |
Andel godkända ansökningar som avser kliniska studier (medicinsk forskning) fördelat på olika ansökningskategorierna (avgiftskategorier) hos Etikprövningsmyndigheten under perioden 2020–2022.
Så är urvalet gjort
Stora delar av den data som presenteras rörande etikprövningsansökningar bygger på ett underlag med ärendeinformation från Etikprövningsmyndighetens diarium. I bearbetningen av underlaget har följande urval och beaktanden gjorts:
- Om inget annat anges i figurtexterna har godkända ansökningar i avgiftskategori A-E (som avser medicinsk forskning), grundansökan del ett för kliniska läkemedels-prövningar (ansökningar som hanteras via den nya förordningen för kliniska läkemedelsprövningar, CTR) och grundansökan för medicinteknik inkluderats. Detta innebär att alla typer av ändringsansökningar har exkluderats, samt grundansökan del två för kliniska läkemedelsprövningar (för att antalet kliniska läkemedelsprövningar ska bli rättvisande för 2022 då ansökan inkommer till Etikprövningsmyndigheten i två delar och hanteras som två olika ärenden). Ansökningar som resulterar i rådgivande yttranden (ca 70 per år) som inte faller under definitionen av forskning i etikprövningslagstiftningen och ansökningar av ärendetyp ”övrig” har också exkluderats.
- För att koppla forskningshuvudman mot sjukvårdsregion för privata vård-givare och företag har huvudkontor eller bolagsadress använts. Dessa ärenden motsvara mindre än 5 procent av det totala antalet ansökningar. För vissa enskilda ärenden är det oklart vem som är ansvarig forskningshuvudman, alternativt att informationen saknas i underlaget. Dessa ansökningar har räknats bort i Figur 3.
Publicerad
Uppdaterad






