Kliniska läkemedelsprövningar som ska genomföras i Sverige kräver godkännande av Läkemedelsverket. Ansökningarna till Läkemedelsverket ger en överblick över antalet kliniska läkemedelsprövningar som planeras i Sverige.
Antal inkomna ansökningar om kliniska läkemedelsprövningar
Läkemedelsverket presenterar regelbundet statistik över antalet inkomna ansökningar (uppgifter från tidskriften "Information från Läkemedelsverket", nummer 4 2015 och Årsstatistik 2022 - kliniska läkemedelsprövningar). Vid jämförelser mellan EudraCT (European Union Drug Regulating Authorities Clinical Trials Database) och Läkemedelsverkets ärendehanteringssystem skiljer sig antal inkomna ansökningar lite åt, men över tid visar de båda källorna likartade trender.
Skillnaderna beror framförallt på att Läkemedelsverkets ärendehanteringssystem inkluderar återansökningar (resubmissions) samt att så kallade VHP-ansökningar (Voluntary Harmonisation Procedure, en process för EU-gemensam bedömning av ansökningar) registreras vid olika tidpunkter hos de nationella läkemedelsmyndigheterna jämfört med den ursprungliga registreringen i EudraCT.
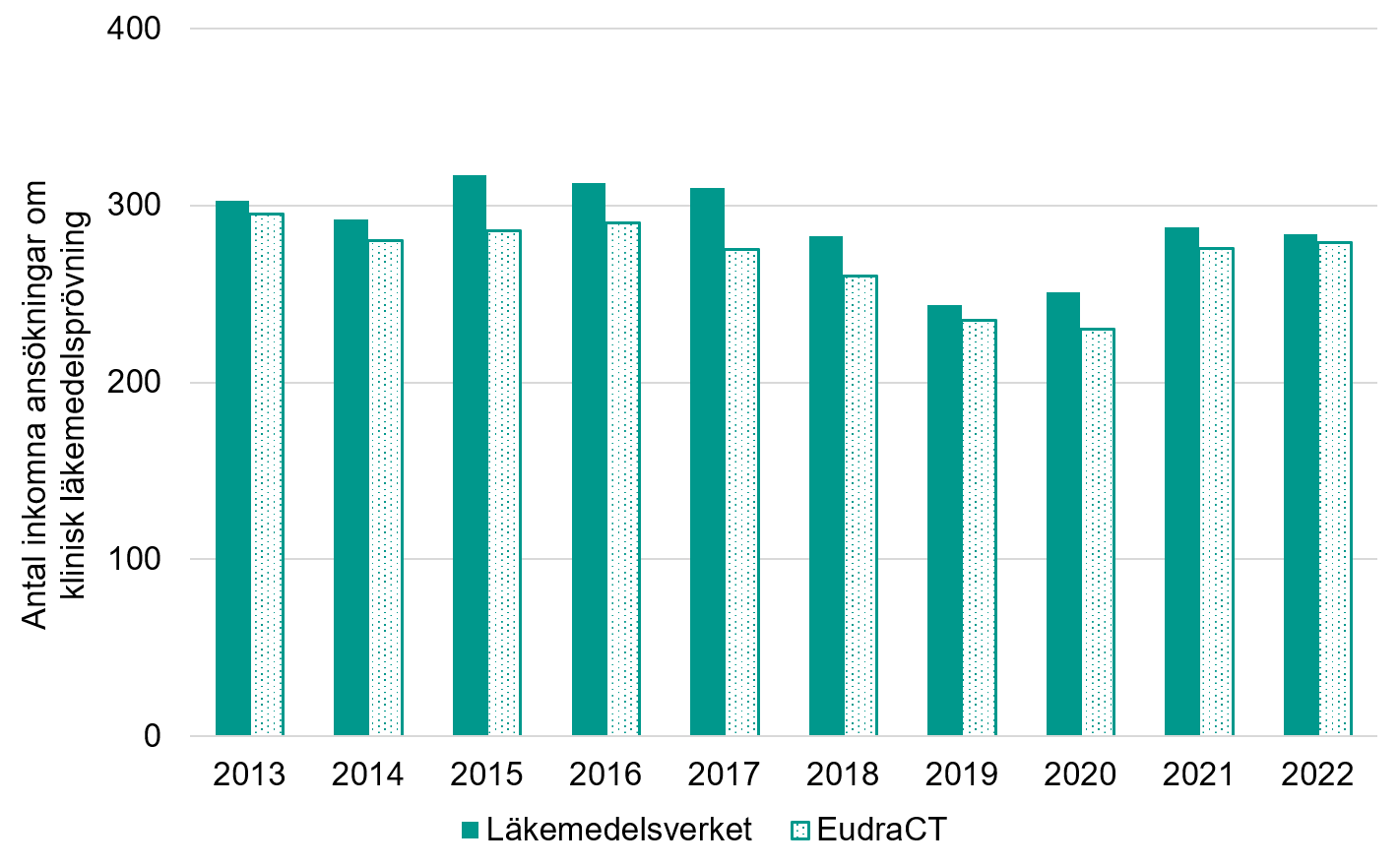
Figur 1. Antal inkomna ansökningar om kliniska läkemedelsprövningar baserat på information från Läkemedelsverkets årsstatistik om kliniska läkemedelsprövningar. För 2022 inkluderar Läkemedelsverket även kliniska läkemedelsprövningar som hanteras via Clinical Trials Information System (CTIS).
Årtal | Läkemedelsverket | EudraCT |
|---|---|---|
2013 | 303 | 295 |
2014 | 292 | 280 |
2015 | 317 | 286 |
2016 | 313 | 290 |
2017 | 310 | 275 |
2018 | 283 | 260 |
2019 | 244 | 235 |
2020 | 251 | 230 |
2021 | 288 | 276 |
2022 | 284 | 279 |
Ansökningar fördelade på kommersiella och akademiska läkemedelsprövningar
Läkemedelsverkets årsstatistik har information om hur antalet ansökningar fördelar sig mellan akademiska och kommersiella kliniska läkemedelsprövningar*. Antalet kliniska läkemedelsprövningar har legat relativt stabilt under den senaste 10-årsperioden, det gäller såvål akademisk som kommersiell sponsor. En viss minskning noteras för kommersiella prövningar under 2019–2020 följt av en återhämtning under 2021–2022. Andelen kommersiella kliniska läkemedelsprövningar är cirka 70 % (medelvärde 2020–2022).
*Begreppen ”industrisponsrade” eller ”företagssponsrade” används ofta synonymt med ”kommersiella” kliniska läkemedelsprövningar. Begreppet ”icke-kommersiell” används på motsvarande sätt synonymt för ”akademiska” kliniska läkemedelsprövningar. Begreppen utgår ifrån den regulatoriska uppdelning av ansvarig sponsor vid ansökan till Läkemedelsverket.
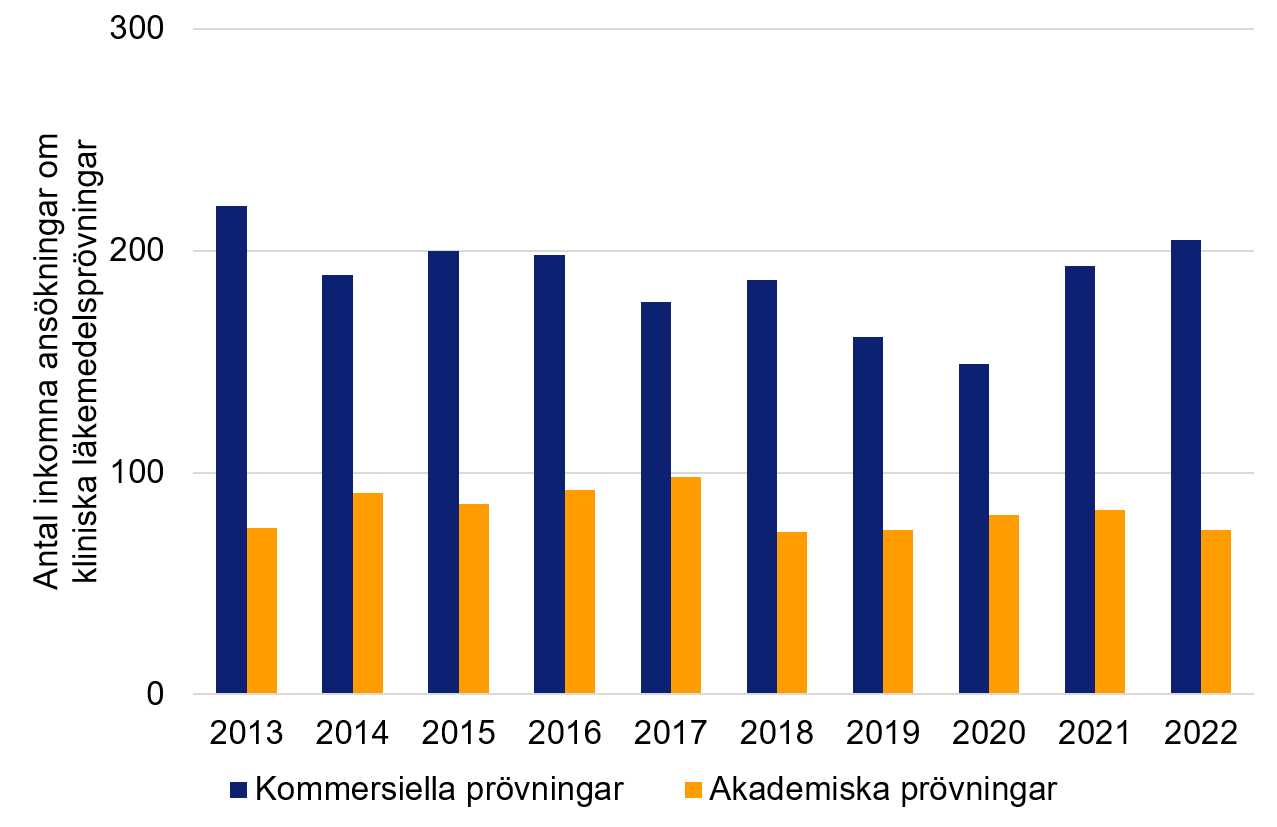
Figur 2. Antal inkomna ansökningar om kliniska läkemedelsprövningar till EudraCT fördelat på sponsortyp: kommersiell respektive akademisk.
Årtal | EudraCT inkomna | EudraCT inkomna |
|---|---|---|
2013 | 220 | 75 |
2014 | 189 | 91 |
2015 | 200 | 86 |
2016 | 198 | 92 |
2017 | 177 | 98 |
2018 | 187 | 73 |
2019 | 161 | 74 |
2020 | 149 | 81 |
2021 | 193 | 83 |
2022 | 205 | 74 |
Kliniska läkemedelsprövningar fördelade på studiefaser
Årsstatistiken från Läkemedelsverket innehåller information om hur ansökningarna för läkemedelsprövningarna fördelar sig på olika studiefaser (Fas I-IV)*. Fördelning är 13 % för fas I, 31 % för fas II, 45 % för fas III och 11 % för fas IV (medelvärde 2020–2022; studier där uppgift om fas saknas är borträknade).
*Beskrivning av de olika studiefaserna i en klinisk läkemedelsprövning. Fas I fokuserar på säkerhet och dosering, fas II utvärderar effektivitet och säkerhet på en större skala, fas III bekräftar resultat i en ännu större och mer varierad population inför myndighetsgodkännande och fas IV innebär eftermarknadsövervakning av läkemedlets effekter när det används i bredare befolkningsgrupper.
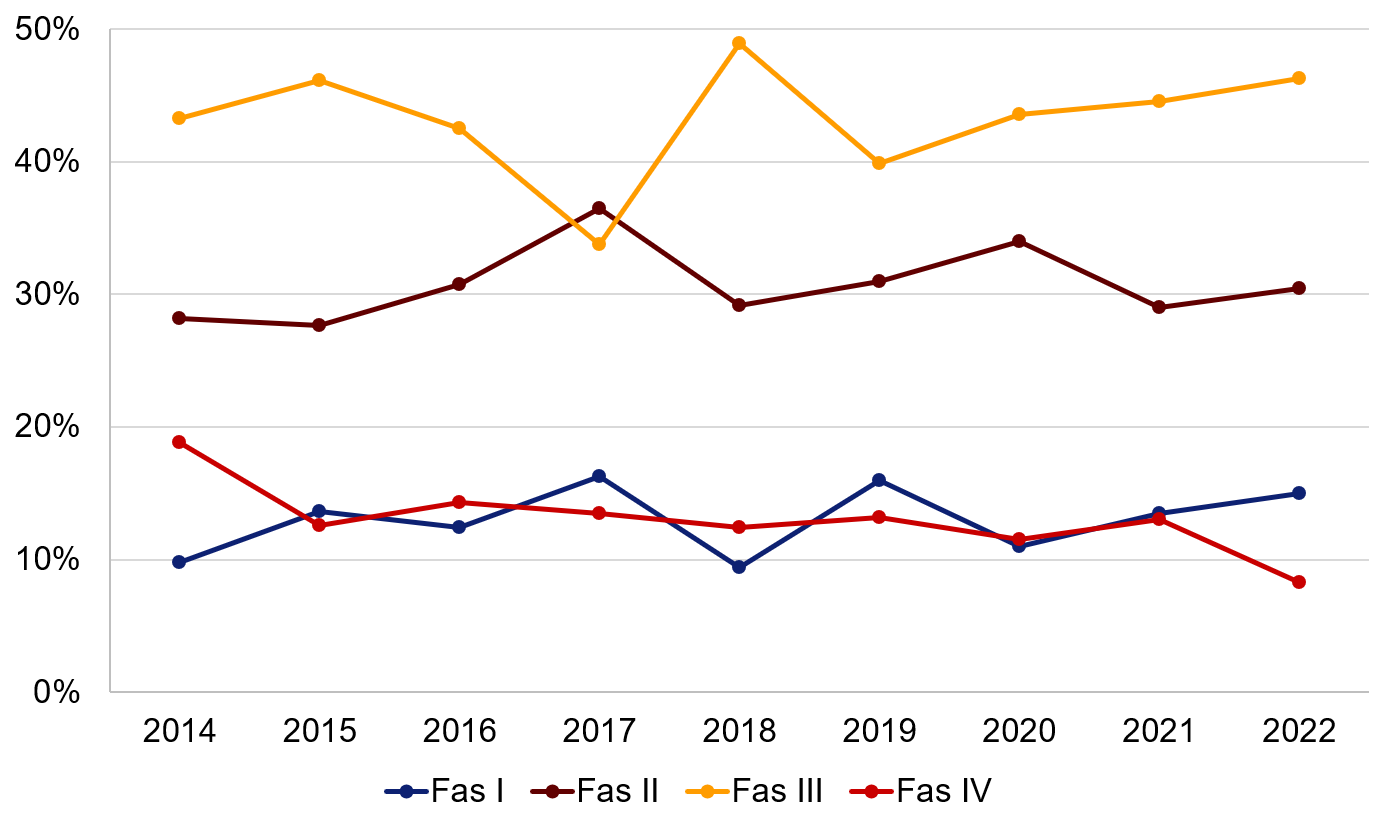
Figur 3. Antal inkomna ansökningar för kliniska läkemedelsprövningar fördelat på olika studiefaser (studier där uppgift om fas saknas är borträknade).
Fas I | Fas II | Fas III | FasIV | |
|---|---|---|---|---|
2014 | 10% | 28% | 43% | 19% |
2015 | 14% | 28% | 46% | 13% |
2016 | 12% | 31% | 42% | 14% |
2017 | 16% | 37% | 34% | 13% |
2018 | 9% | 29% | 49% | 12% |
2019 | 16% | 31% | 40% | 13% |
2020 | 11% | 34% | 44% | 11% |
2021 | 13% | 29% | 45% | 13% |
2022 | 15% | 30% | 46% | 8% |
Andel godkända ansökningar om kliniska läkemedelsprövningar
Ett utdrag från Läkemedelverkets diarium (juni 2023) visar att en stor andel av alla ansökningar blir godkända. 2020–2022 godkändes i snitt 94 procent av ansökningarna. Andel avslag låg på en procent under samma period. Siffran har även tidigare år legat på en till två procent (uppgifter från Läkemedelsverkets tidskrift Information från Läkemedelsverket, nummer 4, 2015). Antalet inkomna ansökningar kan därför antas vara representativt för antalet godkända ansökningar över tid.
Godkänd | Avslag | Annat | |
|---|---|---|---|
2020 | 206 | 2 | 10 |
2021 | 262 | 2 | 3 |
2022 | 238 | 6 | 21 |
Årtalen motsvarar det år som ärendena inkommit till Läkemedelsverket även om beslut ibland tas året efter. Annat beslut innebär oftast att ansökan återtagits eller förfallit eller att beslut ännu inte tagits (för 2022 väntade tre ärenden på beslut i juni 2023).
Mer information om kliniska läkemedelsprövningar
Vetenskapsrådet har sedan tidigare gett ut två rapporter med mer detaljerad information och statistik om kliniska läkemedelsprövningar baserat på utdrag från Läkemedelsverket med data från EudraCT för åren 2010–2018. Rapporterna innehåller bland annat planerat antal forskningspersoner per studie och variationer över tid, geografisk fördelning av prövningar på Sveriges sjukvårdsregioner, åldersfördelning och andel studier där barn deltar som forskningspersoner, visualiseringar av sjukvårds-regionernas deltagande i multicenterstudier, fördelning av antal studier och forskningspersoner på olika sjukdomsområden.
I rapporterna finns också flera jämförelser som visar på skillnader mellan akademiska och kommersiella kliniska läkemedelsprövningar. Exempelvis framgår det att akademiska kliniska läkemedelsprövningar:
- oftast bedrivs i en sjukvårdsregion medan de flesta kommersiella kliniska läkemedelsprövningarna har deltagande kliniker i flera regioner och i andra länder.
- tar längre tid innan de rapporteras som slutförda och inkluderar betydligt fler forskningspersoner per klinik.
Statistik för kliniska läkemedelsprövningar ur ett patientperspektiv Länk till annan webbplats.
Länk till annan webbplats.
Statistik för kliniska läkemedelsprövningar Länk till annan webbplats.
Länk till annan webbplats.
Publicerad
Uppdaterad






